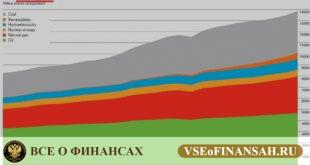
Существует значительная путаница в параметрах удельной теплоты сгорания газов и жидкостей. Связанно это с тем, что исторически жидкости изменяли объёмом — бутылка, бочка, литр. Этот же принцип перешёл на газы — кубометр, литр.
Но теплота сгорания связана с весом (количеством молекул), а не с объёмными характеристиками. Объёмные же характеристики, даже одного и того же вещества, сильно зависят от условий (давление, температура). Проблема усугубляется тем, что выбранные единицы, скажем кубометр/литр и килограмм, имеет близкие значения теплоты сгорания, которые различаются всего на десятки процентов.
Наиболее критическая ситуация сложилась с природным газом.
- Газ имеет разный состав для разных месторождений.
- От месторождения для потребителя газ может менять состав, например, очищаться от тех или иных примесей.
- В паспортах приводится значение для одного килограмма, а потребители получают его кубометрами.
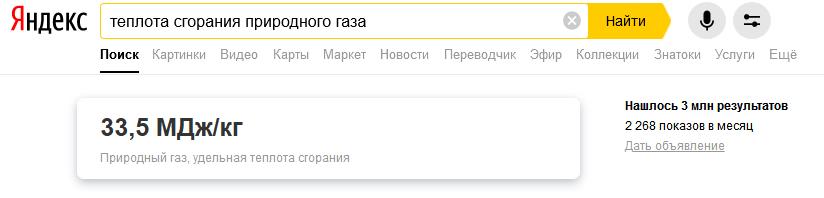
Ситуация настолько серьёзная, что даже Яндекс приводит неправильное значение для теплоты сгорания природного газа 33,5 МДж/кг!
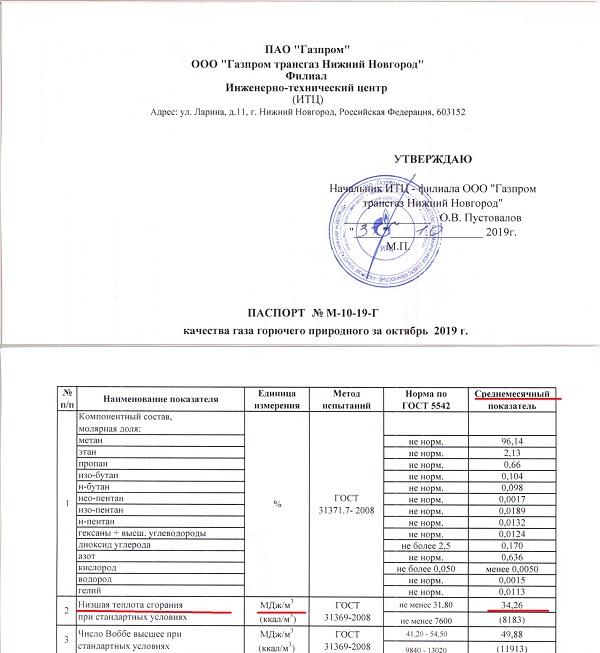
В паспортах на природный газ указано, что такое значение (34,26 Мдж) приблизительно соответствует 1 кубическому метру природного газа!
Как уже выше упоминалось различие может быть обусловлено разным составом газа и разными условиями измерений. Например, у Газпрома температура стандартных условий, как указано в паспорте, является 25° Цельсия, в то время как в физике приняты стандартные условия, когда температура равна 0° Цельсия.
Правильную цифру запомнить очень просто.
Все углеводороды, как следует из названия, это углерод и водород. Углерод имеет теплоту сгорания около 35 МДж/кг. Замещение некоторых атомов углерода, атомами водорода, увеличивают эту цифру, так как хотя атомы водорода в 2,5 выделяют меньше энергии при сгорании, они в 12 раз легче, что даёт почти пятикратный выигрыш в пересчёте на вес!
Самое большое соотношение имеет метан — у него на каждый атом углерода приходится 4 атома водорода. В этом случае удельная теплота сгорания составляет 50 МДж/кг.
А вот объёмные характеристики могут отличаться очень сильно!
© 2019 — 2024, Все о финансах. Все права защищены. Копирование материалов только с разрешения автора.
Самую свежую и актуальную правовую информацию, с учетом индивидуальных нюансов вашей проблемы, можно получить по круглосуточным бесплатным телефонам:
или заполнив форму ниже.
 Все о финансах Юридическая и финансовая консультации
Все о финансах Юридическая и финансовая консультации